Il Paradosso dello Specchio
Vi è mai capitato di osservare una persona dopo un periodo di lutto o di grave crisi e avere la sensazione che sia “invecchiata di dieci anni in una notte”? Quello che ai nostri occhi appare come un cambiamento estetico è, in realtà, l’eco macroscopica di un collasso microscopico. La biologia molecolare moderna ha smesso di considerare la mente e il corpo come entità separate: oggi sappiamo che i nostri pensieri e le nostre sfide emotive dialogano costantemente con il cuore delle nostre cellule.
I protagonisti di questa conversazione sono i telomeri, i “cappucci” protettivi situati alle estremità dei nostri cromosomi. Immaginateli come i puntali di plastica che impediscono ai lacci delle scarpe di sfilacciarsi: senza di essi, la nostra architettura genetica diventerebbe instabile, portando la cellula al disastro. A bilanciare questo logoramento interviene la telomerasi, un enzima straordinario — spesso definito “della giovinezza” — capace di riparare e allungare queste estremità. Comprendere questo meccanismo significa smettere di vedere l’invecchiamento come un processo passivo e iniziare a percepirlo come un sistema dinamico che possiamo, entro certi limiti, influenzare.
——————————————————————————–
Takeaway 1: Lo stress non è solo un’emozione, è un acceleratore cellulare di dieci anni
L’evidenza molecolare è impietosa: lo stress non logora solo i nervi, ma divora fisicamente i nostri cromosomi. Lo studio fondamentale condotto da Elissa Epel e Elizabeth Blackburn (Premio Nobel per la Medicina) ha analizzato donne sane in premenopausa, rivelando che la percezione soggettiva dello stress agisce come un veleno cellulare.
I numeri sono scioccanti. Le donne che percepivano i livelli più alti di stress presentavano telomeri significativamente più brevi: circa 3.110 paia di basi (bp) contro i 3.660-bp del gruppo a basso stress. Considerando che la perdita fisiologica media è stimata tra 31 e 63 paia di basi all’anno, questo divario di 550-bp si traduce in un invecchiamento supplementare di 9-17 anni. Non è solo un dato statistico; è la prova che la nostra mente ha il potere di riscrivere il destino biologico della nostra pelle e dei nostri organi, accelerando il rischio di patologie cardiovascolari e infarti miocardici.
“Numerosi studi dimostrano i legami tra stress cronico e gli indici di cattiva salute… Tuttavia, l’esatto meccanismo di come lo stress si trasforma ‘sotto la pelle’ (under the skin) rimane poco chiaro. Qui forniamo la prova che lo stress psicologico… è significativamente associato con un alto stress ossidativo, inferiore alla telomerasi attiva, e più corta della lunghezza dei telomeri.” — Epel et al., PNAS
——————————————————————————–
Takeaway 2: La “Cronicità” dell’assistenza e il logoramento invisibile
Un altro pilastro della ricerca ha riguardato le “madri assistenziali” (caregivers) impegnate nella cura di figli con malattie croniche. Qui la scienza ci offre una lezione fondamentale sulla resilienza: il fattore determinante per l’invecchiamento precoce non è lo stato di caregiver in sé, ma la durata cumulativa dello stress.
Sebbene nel gruppo delle caregivers esista una correlazione tra l’età del bambino e l’accorciamento dei telomeri (r = -0.45), l’analisi statistica ha dimostrato che la cronicità dello stress (gli anni passati a fornire assistenza) è un fattore predittivo indipendente e molto più potente dell’età cronologica. In altre parole, lo stress cronico agisce come un lento attrito molecolare: più anni di “allarme” vive il sistema nervoso, più i telomeri vengono sacrificati, indipendentemente da quanto siamo giovani sulla carta d’identità. È un avvertimento vitale sulla necessità di gestire il carico mentale a lungo termine prima che diventi un danno strutturale permanente.
——————————————————————————–
Takeaway 3: Il limite di Hayflick e l’orologio molecolare
Perché i telomeri sono considerati il nostro “orologio molecolare”? La risposta risiede nel Limite di Hayflick: le cellule somatiche umane possono dividersi solo un numero finito di volte prima di entrare in senescenza o apoptosi (morte programmata).
L’accorciamento avviene a causa del cosiddetto “end-replication problem”: la DNA polimerasi, l’enzima che copia il nostro codice genetico, non è in grado di completare la replicazione all’estremità 3′ delle molecole lineari di DNA. Ogni divisione “mangia” un pezzetto di telomero. Quando il cappuccio diventa troppo corto, la cellula riceve un segnale di stop definitivo.
Lo stress accelera questo timer attraverso tre percorsi critici:
- Inibizione della telomerasi: lo stress riduce l’attività dell’enzima riparatore, impedendo il “rabocco” dei telomeri.
- Stress ossidativo: l’eccesso di radicali liberi danneggia direttamente le sequenze telomeriche (TTAGGG).
- Compromissione immunitaria: accelera la senescenza dei leucociti, rendendoci biologicamente più vecchi e vulnerabili alle infezioni.
——————————————————————————–
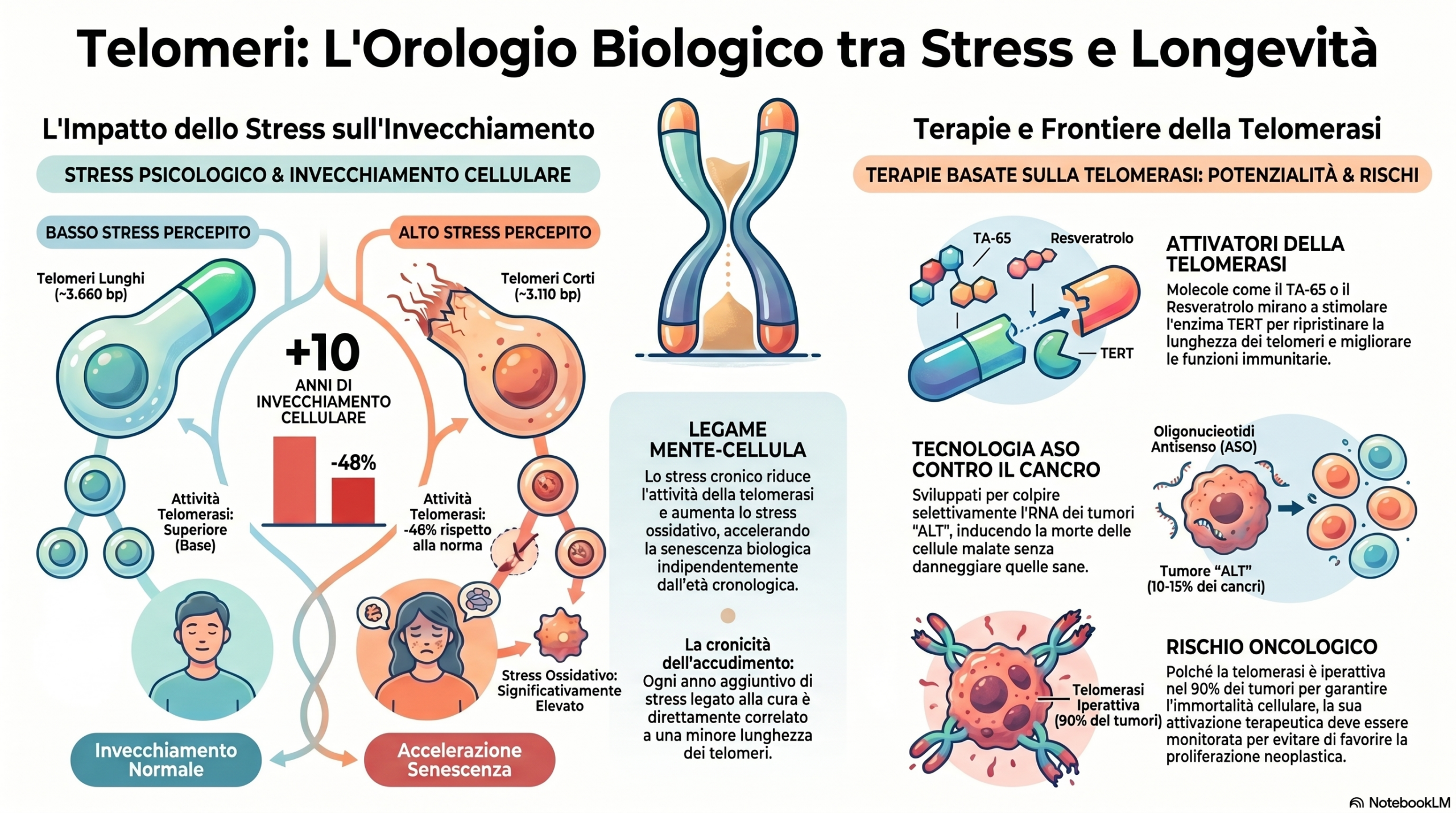
Takeaway 4: Attivatori della Telomerasi – Tra promesse di eterna giovinezza e rischi oncologici
La ricerca sulla longevità ha identificato diverse molecole capaci di stimolare la telomerasi e potenzialmente rallentare l’orologio cellulare. Tra i più studiati troviamo:
- TA-65: un estratto purificato della radice di Astragalus membranaceus.
- EGCG (Tè verde), Resveratrolo e Vitamina D: composti che modulano indirettamente l’ambiente cellulare favorendo la stabilità dei telomeri.
Tuttavia, l’attivazione indiscriminata richiede una cautela scientifica estrema. Esiste infatti il “paradosso del cancro”: l’85-90% delle cellule tumorali riattiva prepotentemente la telomerasi per diventare immortale e replicarsi all’infinito. La sfida della medicina moderna è imparare a proteggere le cellule sane senza fornire, involontariamente, la chiave dell’immortalità a quelle malate.
——————————————————————————–
Takeaway 5: La nuova frontiera – Colpire i telomeri per “accecare” i tumori intrattabili
Nel 2023, una scoperta rivoluzionaria dell’IFOM di Milano ha trasformato i telomeri da scudo della cellula a “tallone d’Achille” del cancro. I ricercatori si sono concentrati sui tumori ALT (Alternative Lengthening of Telomeres), forme estremamente aggressive come il glioblastoma e l’osteosarcoma, che non usano la telomerasi ma un meccanismo alternativo per mantenere i propri telomeri sempre “danneggiati” e attivi.
La chiave di volta è una specifica famiglia di RNA telomerici, definiti “RNA di allarme”, che queste cellule producono per promuovere la propria riparazione e sopravvivenza. Utilizzando la tecnologia degli oligonucleotidi antisenso (ASO), gli scienziati sono riusciti a creare “farmaci molecolari” che bloccano selettivamente questi RNA. Il risultato? La cellula tumorale viene “accecata”, perde la capacità di riparare i propri telomeri e collassa, morendo per senescenza indotta, mentre le cellule sane rimangono intatte. È una frontiera di precisione millimetrica che apre speranze concrete per i tumori finora considerati intrattabili.
——————————————————————————–
Conclusione: Oltre la biologia, una scelta di vita
Le scoperte sui telomeri ci consegnano un messaggio potente: la nostra biologia non è un destino immutabile scritto nel marmo, ma un sistema dinamico in costante risposta al nostro stile di vita e alla nostra percezione della realtà. Se i telomeri sono i biomarkers della nostra salute cellulare, noi siamo — in parte — i custodi del loro tempo.
Se potessi vedere il tuo orologio molecolare ticchettare oggi stesso, cambieresti il modo in cui rispondi alla prossima sfida della tua giornata? La consapevolezza che “la mente parla alle cellule” non è solo scienza: è l’opportunità di riprendere il controllo sul proprio invecchiamento, una cellula alla volta.






